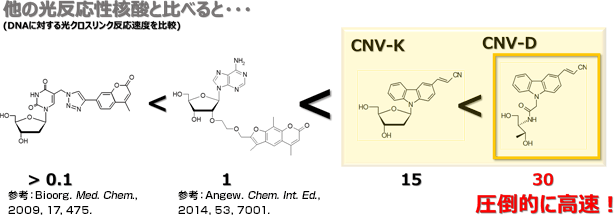
光架橋性人工核酸 CNVシリーズ
精密有機合成の知見をライフサイエンスの分野へ
日華化学では、遺伝子工学に技術革新をもたらす「DNA光操作システム」の事業化に取り組んでいます。
従来、DNAの編集・操作は煩雑な酵素法や化学反応で行われていましたが、北陸先端科学技術大学院大学 藤本教授が発明したCNVシリーズ(CNV-KおよびCNV-D)をDNAに組み込むことで、光を用いて自由自在にDNAを操作することができます。このユニークな性質を用いた研究は学術的に高く評価され、先端医療だけでなく、ケミカルバイオロジー、ナノテクノロジー、環境分野などへの応用が可能です。
当社は、この技術に着目し、藤本教授らと共同研究を重ねた結果、当社のコア技術である精密有機合成の知見を生かし、本試薬の工業スケールでの安定供給・品質の確保を実現しました。
今後成長が期待されるライフサイエンス分野において、さらなる貢献を果たすことを目的に、CNVシリーズをDNA/RNA合成試薬、および修飾オリゴ核酸として販売を開始することにしました。なお、オリゴ核酸合成は、北海道システム・サイエンス社と業務提携して行っています。
遺伝子診断(コメの品種判定)
現在では、ヒトのゲノムDNAも解読・解析できるようになり、個人がどのような遺伝子を持っているのかを知ることができるようになりました。
光架橋性人工核酸を用いた遺伝子診断は、他の手法と比較しても、操作が簡便で正確性に優れています。
たとえば、コメの品種も特定の遺伝子に対する検査を行うことで簡便に判定でき、食品偽装を防ぐことができます。
植物・動物・細菌・ヒト・・・あらゆる生物への応用も可能です。

感染症の体外診断キット
感染症や遺伝病に特異的なDNA/RNAマーカーに対し、CNVシリーズを用いることで、迅速・簡便かつ正確性に優れた病気の体外診断を行うことができます。

核酸医薬による治療
核酸医薬品はDNAやRNAの配列を認識し、好ましくない遺伝子の働きを阻害します。がんなどの、これまで治療が困難であった病気に対する克服法として期待されています。
上記の例以外にも、光架橋性人工核酸の性質を利用した様々な用途が考えられます。

修飾オリゴ核酸合成
業務提携先の北海道システム・サイエンス社の協力のもと、CNVシリーズを挿入した光架橋性オリゴDNA/RNAを提供しております。CNVシリーズを挿入したオリゴDNAに対する各種修飾も可能です。標準的な納期はおよそ2週間ですが、修飾内容により変更になります。納期・価格など具体的な内容については、お問い合わせください。
| 対応塩基数 | 11mer ~ 50mer |
|---|---|
| 合成スケール | 0.2μmol ~ 1μmol |
| 精製 | 各種精製可能 (HPLC精製、イオン交換精製) |
| CNVシリーズ挿入 | 複数個所挿入の場合はご相談ください |
| 各種修飾 | 5-メチル-dC、2'-Fluoro-RNA挿入、ウラシル(dU)挿入、イノシン挿入など可能です。ご確認ください。 |
製品紹介・応用例
可逆的な光クロスリンク反応を行う人工核酸
北陸先端科学技術大学院大学藤本教授が開発したCNVシリーズを含むオリゴ核酸は、わずか数秒のUV光照射により、相補的な配列をもつ核酸と光架橋し、通常の乖離条件下では1本鎖に戻ることの無い強固な2重鎖核酸構造を形成します。従来の酵素によるDNA/RNA操作が抱える問題を解決できます。
現在CNVシリーズは、基本骨格が異なる2種類をラインナップしております。
【第一世代】DNAと同じデオキシリボースを基本骨格とするCNV-K
【第二世代】D-トレオニノールを基本骨格とすることで性能がアップしたCNV-D
上記2種に関して、ホスホロアミダイト体および修飾オリゴ核酸として提供しております。
CNVシリーズは・・・
- 366nmのUV照射でピリミジン塩基と100%架橋
- 312nmで可逆的に乖離可能
- DNAだけでなくRNAに対しても操作可能
- UVの波長と照射時間により架橋率をコントロール
- 光架橋のスイッチングのタイミングや場所を限定できる
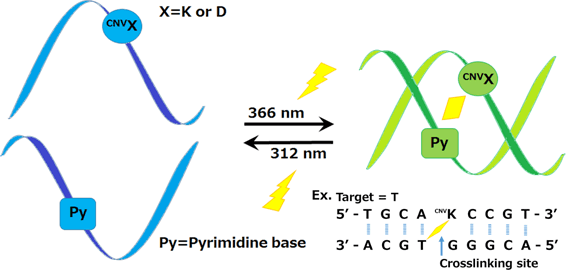
CNVシリーズを組み込んだオリゴDNAによる光架橋
主な特徴
核酸の光架橋
CNVシリーズ含有オリゴDNAは366nmの光照射により、
1秒で相補鎖のチミン(シトシンは25秒)と共有結合([2+2]光環化)を100%形成
- CNV-KまたはDから見て、5'側へ隣の塩基と水素結合しているピリミジン塩基と架橋します。
- 相補部位においてピリミジン塩基とプリン塩基とを識別(プリン塩基とは架橋反応しません。)
- 312nmの光照射を1分間行うことで、架橋が開裂
- どちらの波長も、重大なDNA損傷を引き起こす可能性は低く、また、架橋部位の両側の配列が異なることによる光架橋への影響はほぼありません。
参考:Org. Lett., 2008, 10, 3227-3230
参考:ChemBioChem, 2010, 11, 1661-1664
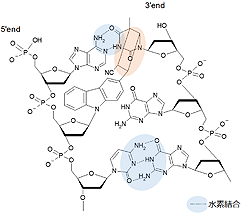
CNV-Kとチミンとの[2+2]光環化
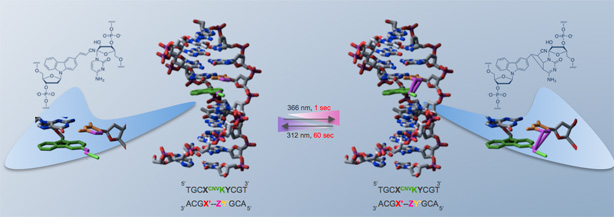
DNA2本鎖でのCNV-Kによる光架橋
シトシンの光交換反応
DNAおよびRNAに対して変異を人工的に導入する方法のうち、DNA中のシトシンをウラシルに変換する方法としてバイサルファイト処理が報告されていますが、ピンポイントでの操作が難しいことやDNAの分解が問題となります。
CNVシリーズの光架橋反応を利用し、核酸中の特定のシトシン(dC)をウラシル(dU)へ変異させることが可能
- CNVシリーズを含むオリゴDNAが相補鎖のdC塩基と架橋
- 2本鎖を90℃で3.5時間加熱
- 相補鎖のdCの脱アミノ化反応が誘導される
-
CNVシリーズと共有結合しているシトシンがウラシルに変換
続けて312nmの光照射を行うことで、dCはdUに変換されたまま、架橋した核酸は開裂します。
この変換はCNVシリーズと架橋したdC塩基にのみ行われ、近接したdC塩基への影響はありません。
参考:ChemBioChem, 2009, 10, 1473-1476
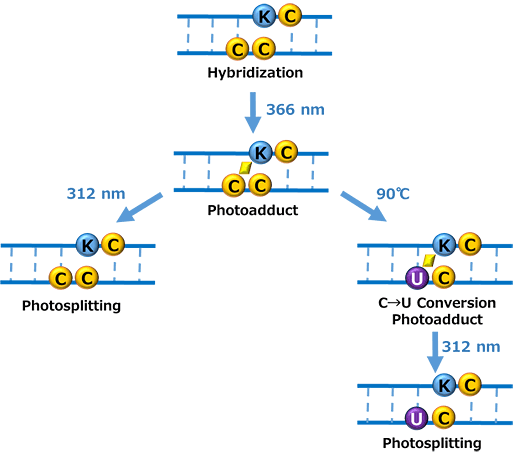
DNAにおけるシトシンからウラシルへの光交換反応
応用実験例
細胞内での遺伝子発現制御(アンチセンス法)
細胞内において、CNV-Kを含むプローブを用いたアンチセンス効果により、遺伝子発現を制御することができます。光照射により、細胞中に取り込まれたプローブが相補部分と架橋し、その遺伝子の翻訳をブロックします。UV照射後、GFP-HeLa細胞内でGFP発現量が抑制されたことが、共焦点顕微鏡により確認されています。
参考:Biomaterials Science, 2014, 2, 9, 1154 -1157
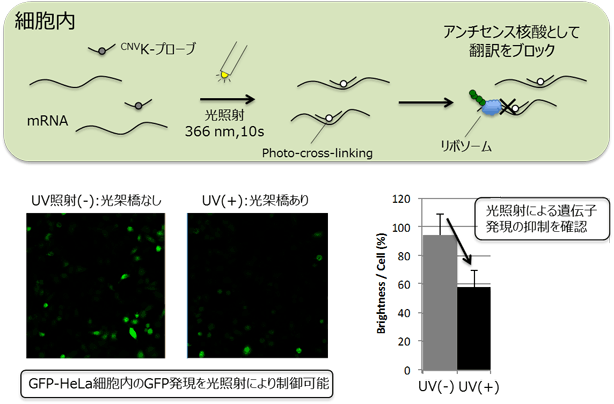
アンチセンス法へのCNV-Kの適応
遺伝子検出(FISH法)
CNV-Kを用いたFISH法による遺伝子の検出は、高次構造を形成している核酸に対しても有効です。一般的なプローブでは高次構造を形成する核酸を検出することは困難です。CNV-Kを含むプローブを用いることで、高次構造に入り込んで光架橋し、通常のプローブでは検出できない核酸の検出も可能です。
参考:Bioorg. Med. Chem. Lett., 2016, 26, 5312-5314
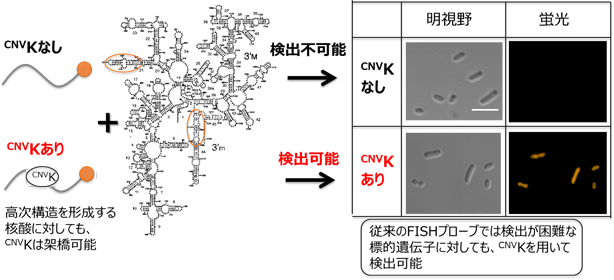
高次構造を持つ核酸のCNV-Kプローブを用いた検出
第一世代光クロスリンカー:CNV-K
製品名 CNV-K phosphoramidite
| Name | CNV-K phosphoramidite |
|---|---|
| Synonyms | 5'-O-(4,4'-Dimethoxytrityl)-1'-(3-cyanovinylcarbazol-9-yl)-2'-deoxy-β-D-ribofuranosyl-3'-[(2-cyanoethyl)-(N,N-diisopropyl)]-phosphoramidite |
| Formula | C50H53N4O6P |
| M.W. | 836.95 |
| CAS No. | 1157899-72-3 |
| Purity by HPLC | > 99% |
| Package | 250mg |
| Freezer storage | -20 to -80℃, dry and dark place |
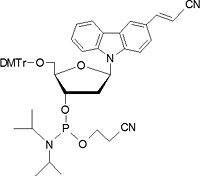
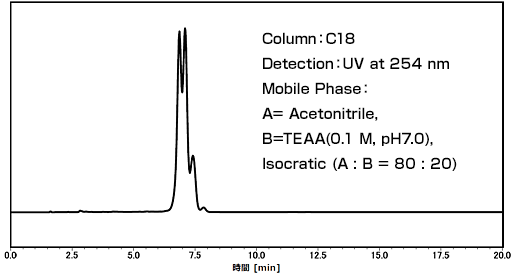
CNV-Kホスホロアミダイトの典型的なHPLCチャート
第二世代光クロスリンカー:CNV-D
製品名 CNV-D phosphoramidite
CNV-Kを凌駕する世界最速のDNA光架橋素子!
| Name | CNV-D phosphoramidite |
|---|---|
| Synonyms | 3-O-(4,4'-Dimethoxytrityl)-2-N-(N-carboxy-3-cyanovinylcarbazol)-D-threonin-1-yl-O-[(2-cyanoethyl)-(N,N-diisopropyl)]-phosphoramidite |
| Formula | C51H56N5O6P |
| M.W. | 865.99 |
| CAS No. | N/A |
| Purity by HPLC | > 99% |
| Package | 250mg |
| Freezer storage | -20 to -80℃, dry and dark place |
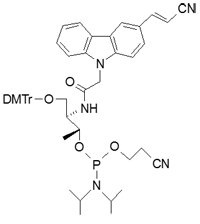

CNV-Dホスホロアミダイトの典型的なHPLCチャート
CNV-Kよりも圧倒的に反応が速い次世代人工核酸
光架橋の反応部である3-シアノビニルカルバゾールはそのままに、基本骨格をD-トレオニノールに変更することで、基本的な性質はCNV-Kと同様でありながら、より速く、より正確に光架橋を行います。
第一世代のCNV-Kの2~8倍の光反応性!
CNV-Kの応用例に置き換え可能!
- D-トレオニノールのフレキシブルな構造により、2本鎖中での光架橋が効率化。
- チミンとシトシン、それぞれとの架橋に必要なUV照射時間がほぼ同じになります。
- CNV-DはCNV-Kと同様の操作を行うことができ、特に条件や制限はありません。
- CNV-Dを組み込んだオリゴ核酸の合成は、 CNV-Kと同様に行うことができます。
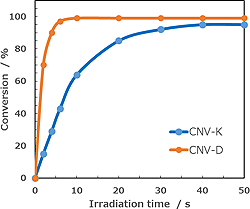
参考および改変:Org. Lett. 2015, 17, 936-939